

发布时间:2023-12-19 浏览次数:7536
近日,深圳格拉布斯研究院双聘教授谭斌团队在亚胺极性反转领域取得了重要突破。研究成果以“有机催化芳构化促进的亚胺极性反转反应(Organocatalytic aromatization-promoted umpolung reaction of imines)”为题在《自然化学》(Nat. Chem.)上发表。
俗话说:“男追女,隔座山;女追男,隔层纱。”这是对恋爱中的反转的形象比喻。同样化学中的反转也与恋爱中的反转一样,其本质就是一个活化能降低的过程。原本活化能很高很难发生的反应发生反转后活化能变低则反应就很容易进行。
在化学领域,极性反转(umpolung)是指某结构或官能团经过某些转化后电性变得与原来的相反。发生极性反转后的中间体可以发生原结构(或官能团)本不可能发生的反应:比如只能发生亲核反应的官能团,经极性反转后可以发生亲电反应。
亚胺是有机化学中十分重要的官能团,是化学和生物合成胺类化合物的一类应用广泛的有机前体。正常情况下亚胺碳氮双键中的碳在化学反应中只作为亲电位点参与反应同时氮只作为亲核位点参与反应。而发生极性反转后的亚胺碳氮双键中的碳转变为富电子性从而作为亲核位点参与反应,这样发生极性反转后的亚胺可与各种各样的亲电试剂反应,为高效合成传统合成方法难以得到的目标化合物提供了新的机会和途径。到目前为止,关于发生极性反转的亚胺碳氮双键中的碳作为亲核位点参与反应的报道较多。与之形成鲜明对比的是,关于发生极性反转的亚胺碳氮双键中的氮作为亲电位点参与反应特别是手性反应的报道却极少且极性转换的效率很低,通常需要强亲核试剂才能与之反应。(图1)。
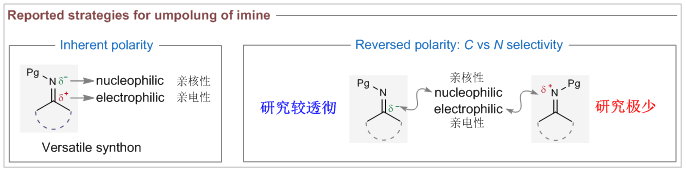
图1:亚胺的固有极性和极性反转
基于上述背景,谭斌讲席教授团队设计了三类N-亲电芳香前体,其在磷酸催化下均能与芳烃或杂芳烃发生极性反转反应高效构建N-芳基化合物、手性氨基化合物、轴手性芳基酰胺和杂芳基酰胺(图2)。为了进一步理解反应过程,作者与加州大学洛杉矶分校Kendall N. Houk教授合作通过DFT计算对反应的机理进行了深入的研究,理论计算表明该过程为离子型机理同时芳构化是实现该策略的重要驱动力。
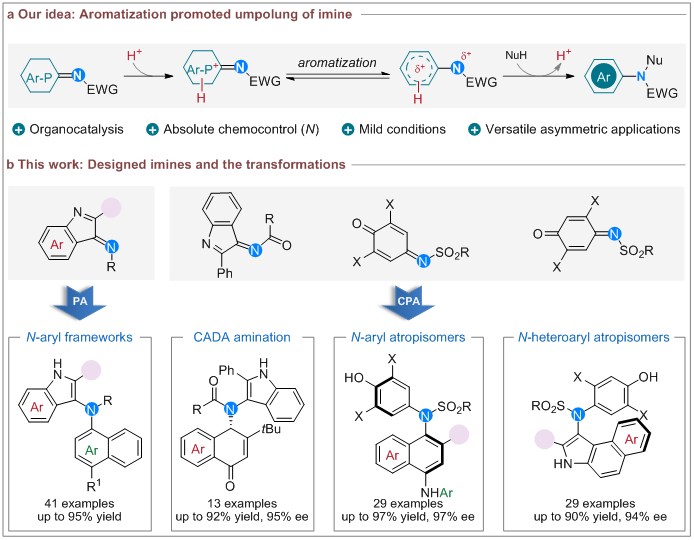
图2:通过芳构化驱动的亚胺极性反转反应高效构建N-芳基化合物、手性氨基化合物、轴手性芳基酰胺和杂芳基酰胺
谭斌讲席教授为论文第一通讯作者,南方科技大学为论文第一通讯单位。合作通讯作者包括加州大学洛杉矶分校Kendall N. Houk教授。该研究项目得到了国家自然科学基金委、广东省广创团队和南科大等项目和单位的大力支持。
原文链接 Chen, YH., Duan, M., Lin, SL. et al. Organocatalytic aromatization-promoted umpolung reaction of imines. Nat. Chem. (2023).
https://doi.org/10.1038/s41557-023-01384-x
https://www.nature.com/articles/s41557-023-01384-x