

发布时间:2025-11-26 浏览次数:1752
手性是自然界的基本属性。从药物与受体的精准识别,到蛋白质折叠、生物信号传递,再到光电器件中对偏振光的选择性响应,手性都发挥着关键作用。近年来,随着细胞识别、精准诊断与活体成像需求的迅速提升,能够在分子层面呈现手性识别的荧光探针受到越来越多的关注。然而,构建结构明确且性能可调的手性荧光分子库依然面临设计和合成的挑战,尤其是在接近生物窗口的红光和近红外区域。
近红外区间的光在生物组织中的散射小、吸收低、背景弱,是实现深层、高对比度成像的关键波段。在诸多NIR发色团体系中,BODIPY以其高度稳定、结构可修饰、量子产率高等优势脱颖而出,并在光诊疗、光子学材料、活体成像等领域展现出独特地位。然而,传统BODIPY结构多集中在可见光范围,难以满足深层组织成像的需求。如何在保持其光学优势的同时,赋予其硼中心手性,并实现其体系化的构建与应用,一直以来缺乏有效的手段。
深圳格拉布斯研究院双聘教授何川课题组近日在Nat. Commun.报道了一项精准可调的不对称催化合成策略,用于系统构建具有近红外光学活性的硼手性BODIPY染料库。该策略通过催化不对称交叉偶联,对前手性BODIPY进行功能化,获得共轭程度更高的染料,并呈现优异的对映体纯度以及可调控的光物理性质。
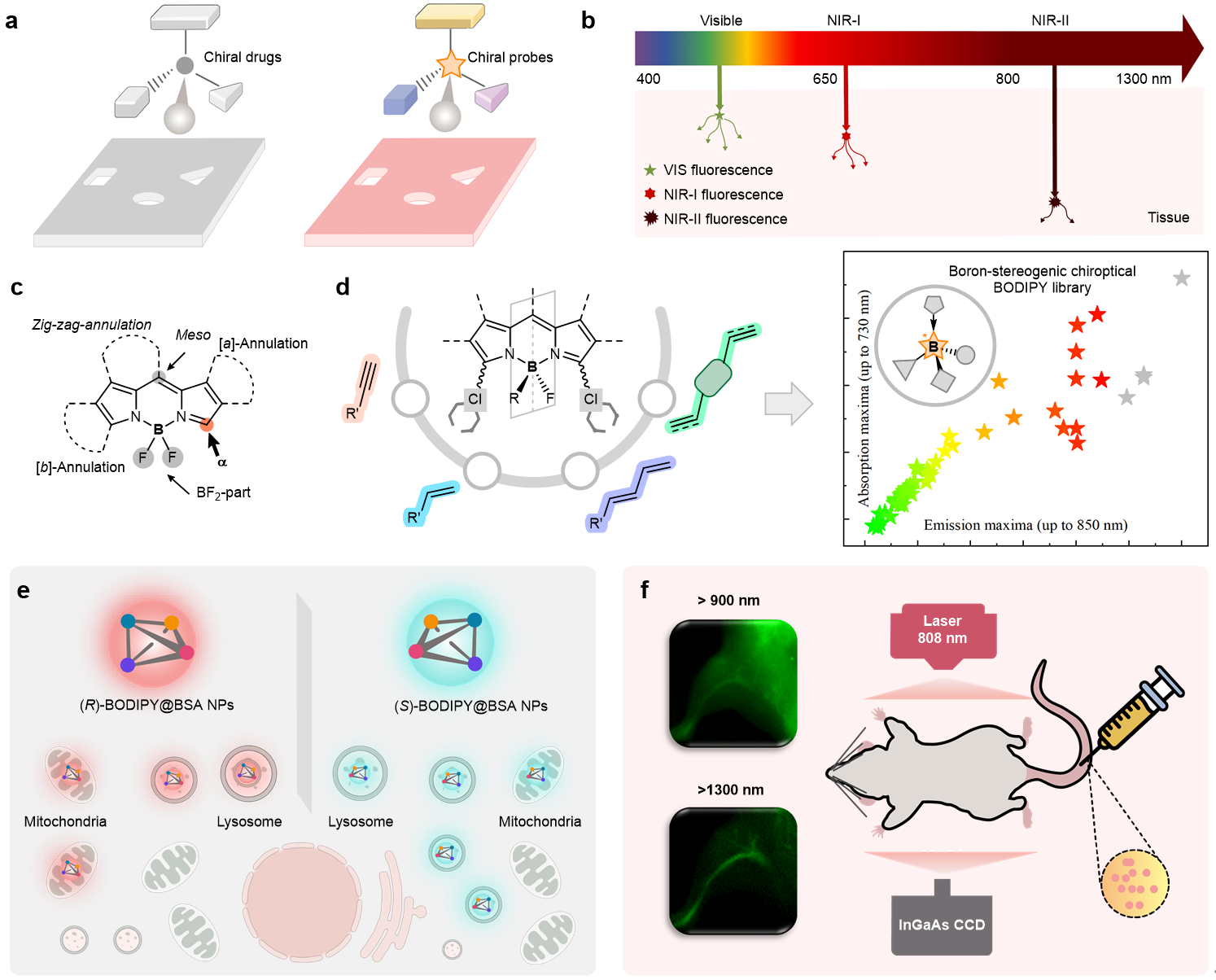
图 1 红光/近红外硼手性BODIPY染料设计策略
该研究围绕硼手性 BODIPY 染料的分子设计,系统构建了两类关键结构:α-炔基与α-烯基硼手性BODIPY。首先,作者以具有两个α C–Cl键的前手性BODIPY 1a为底物,通过系统筛选配体、碱和溶剂,最终确定使用兼具轴手性和中心手性的膦酰胺配体L、CsOAc及TBME可高效实现不对称Sonogashira偶联,在4小时内即得到3a,产率达96%,对映选择性高达99%。在优化条件下,多种芳基炔、杂芳基炔及烷基炔均顺利参与反应,为手性BODIPY体系带来广泛的结构多样性,从而获得不同波长范围的BODIPY荧光团。其中,含吸电子或给电子基团的芳基炔均表现出良好的兼容性;含有OMe、NMe2、NPh2等强给电子基团的炔基表现出显著的红移发射,成功拓展至近红外区域(最高达751–798 nm)。同时,通过改变BODIPY骨架结构或硼中心取代基(如以噻吩取代苯环),也能进一步延伸共轭体系并增强红移效果。由此构建的α-炔基硼手性BODIPY系列覆盖从可见光到近红外的广泛发射范围。
在此基础上,研究团队进一步开发了高效合成α-烯基硼手性BODIPY的方法。将反应体系使用的碱更换为三乙胺后,前手性底物1a可与多类烯烃经历高效的不对称Heck偶联,得到高ee的α-烯基BODIPY(5a–5w)。无论是含酯、酰胺、醚、硅烷等官能团的烯烃,还是芳基烯烃、稠环烯烃及多种共轭二烯体系,都表现出优异兼容性。芳基烯烃及强给电子取代的烯烃(如N,N-二甲基苯乙烯)的发射波长均显著红移,其中5w的发射峰达到730 nm。通过引入杂芳环以及稠环结构(如卡唑、萘基、噻吩等),发射波长可进一步延长,实现近红外手性BODIPY染料构建。
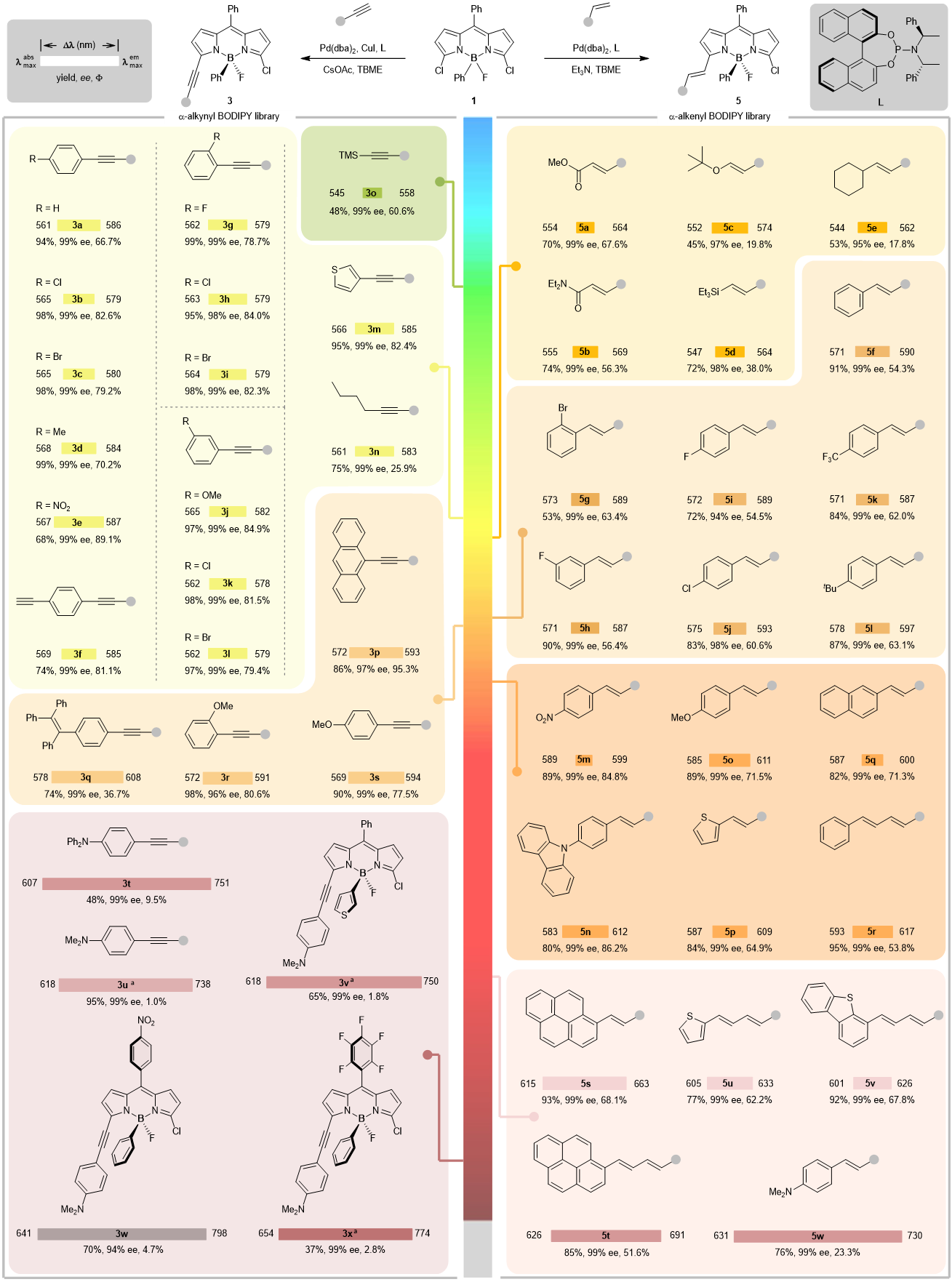
图2 硼手性荧光染料库的高效构建
为进一步红移所得硼手性BODIPY的吸收与发射波长,并展示该体系的结构扩展潜力,作者对α-氯取代的BODIPY进行了多种立体专一的功能化转化。首先,具有不同meso芳基的二氯 BODIPY可顺利经历串联炔基化和烯基化反应,高效构筑3,5位置双取代的手性 BODIPY产物6a-6e,具有优良的对映选择性和显著红移的近红外发射(750-850 nm)。值得一提的是,这些在两个α位引入不同的炔基、烯基或二烯基的结构在此前均难以获得,该方法实现了它们的快速合成。此外,作者成功制备了由1,4-双炔基苯或双烯基苯桥连的BODIPY二聚体6f和6g,具有 99% ee和超过20:1的优异非对映选择性。这类独特的二聚结构在荧光成像中具有较高应用潜力。进一步地,作者利用含三甲基硅基的6b与含有生物活性分子结构单元(如D-葡萄糖苷和维生素E)的叠氮化物进行铜催化的点击反应,顺利获得手性BODIPY三氮唑衍生物6h和6i,产率良好且具有优异的非对映选择性。这一结果表明,经该方法构筑的硼手性BODIPY不仅具备结构可调控,也有望在生物成像与荧光标记等领域发挥作用。
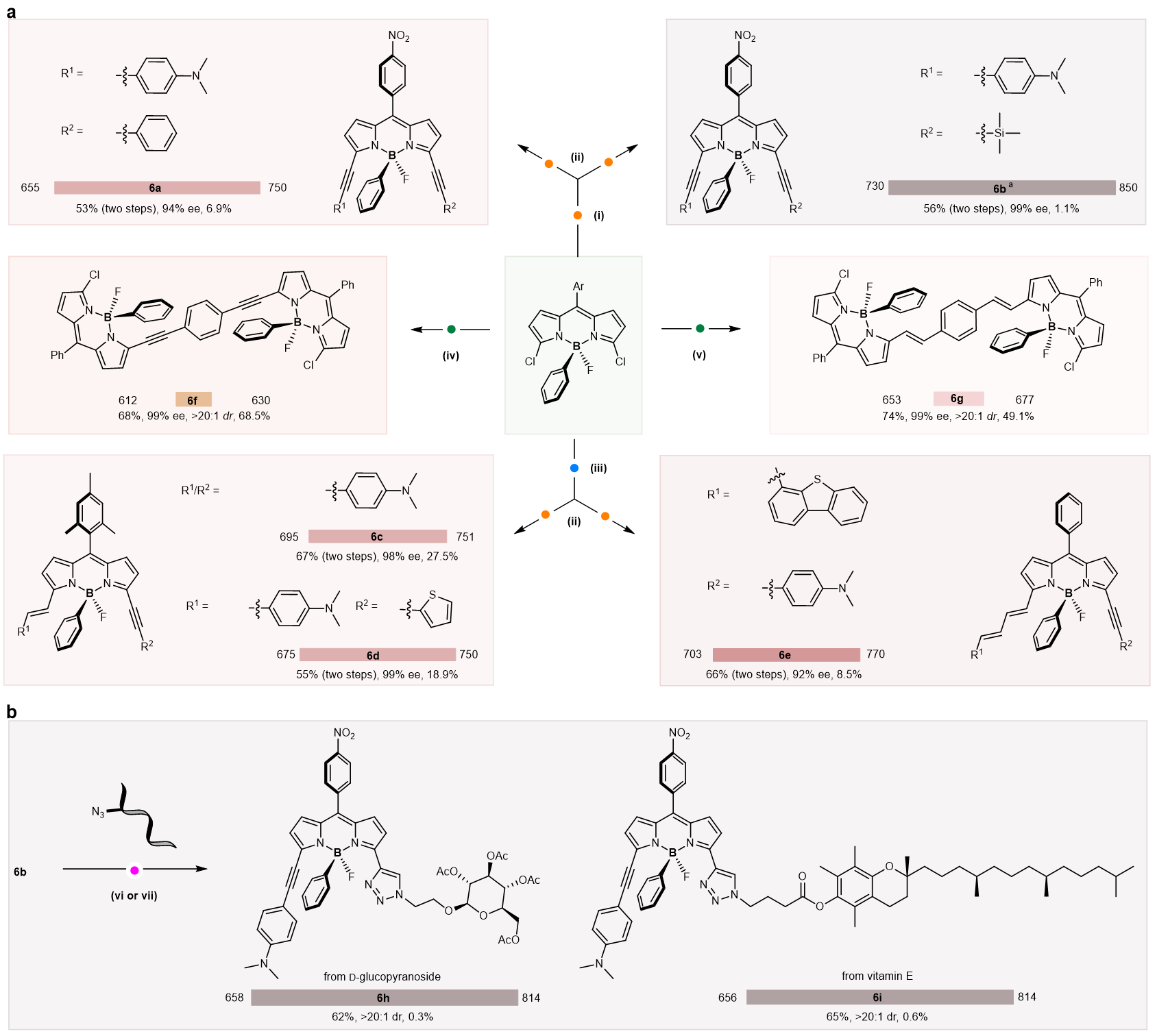
图3 硼手性荧光染料的立体专一性衍生化
为探究硼手性中心对成像行为的影响,作者进一步开展了细胞器共定位实验。利用MitoTracker Green与LysoTracker Red对两个对映体进行分析,结果显示S-3w@BSA对溶酶体具有显著偏向性,其与LysoTracker Red的PCC达到0.896,明显高于其线粒体共定位程度(PCC = 0.492)。相比之下,R-3w@BSA 在溶酶体与线粒体中的共定位程度相近,说明手性可显著影响染料对细胞器的亲和性。
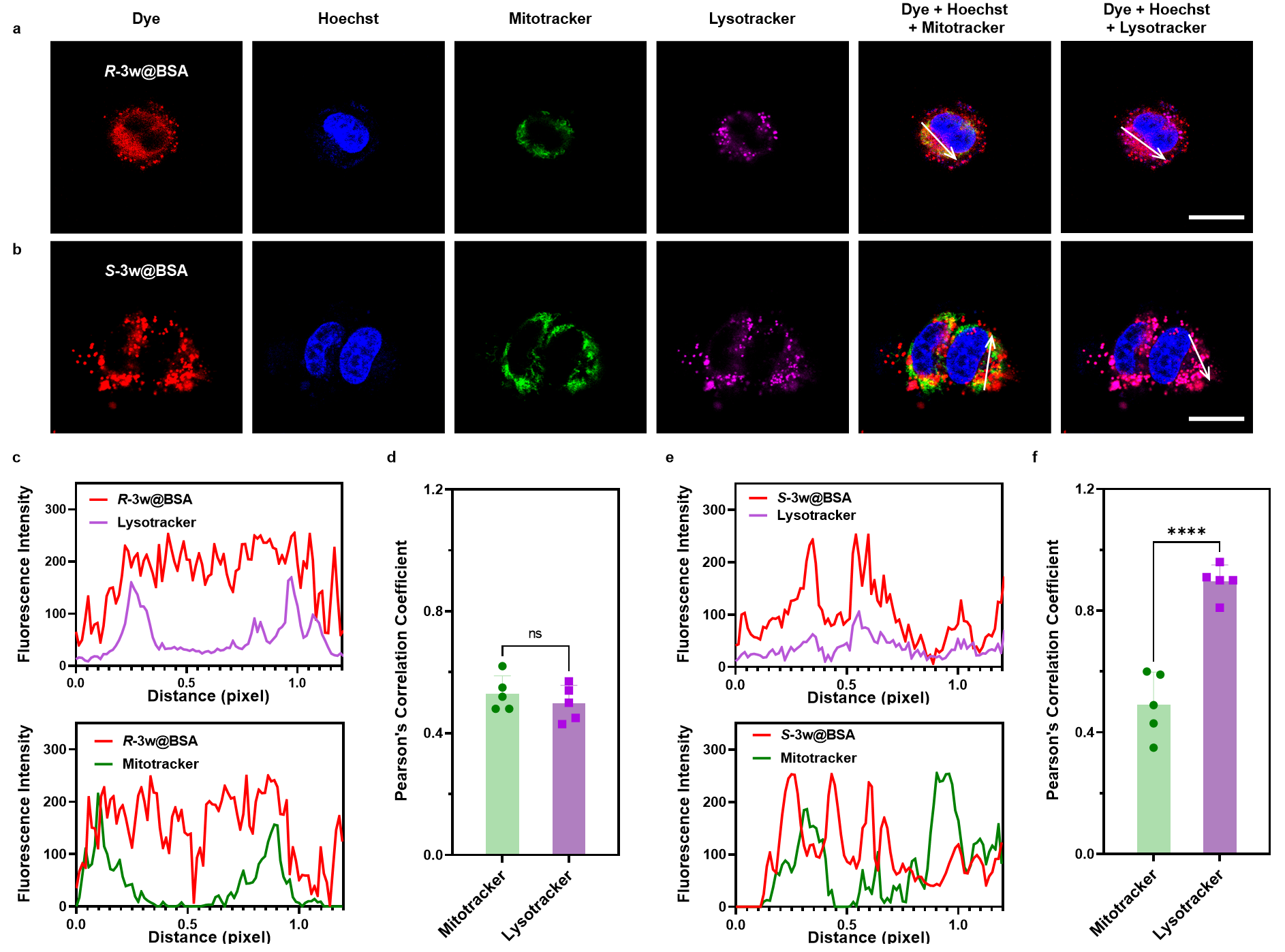
图4 硼手性BODIPY细胞成像
此外,该研究还系统评估了硼手性BODIPY在近红外二区成像中的性能。与临床常用的ICG相比,BODIPY探针在组织模拟环境中表现出更强的穿透深度、更高的成像分辨率与更优的信噪比。体内实验显示,6c@BSA能实现清晰的全身及局部血管成像,尤其在大于一千三百纳米窗口中背景极低。生物分布与组织学分析进一步证明了其良好的生物相容性。整体而言,这类手性 BODIPY探针兼具了优异光学性能与生物选择性,为靶向近红外成像提供了新的可能性。
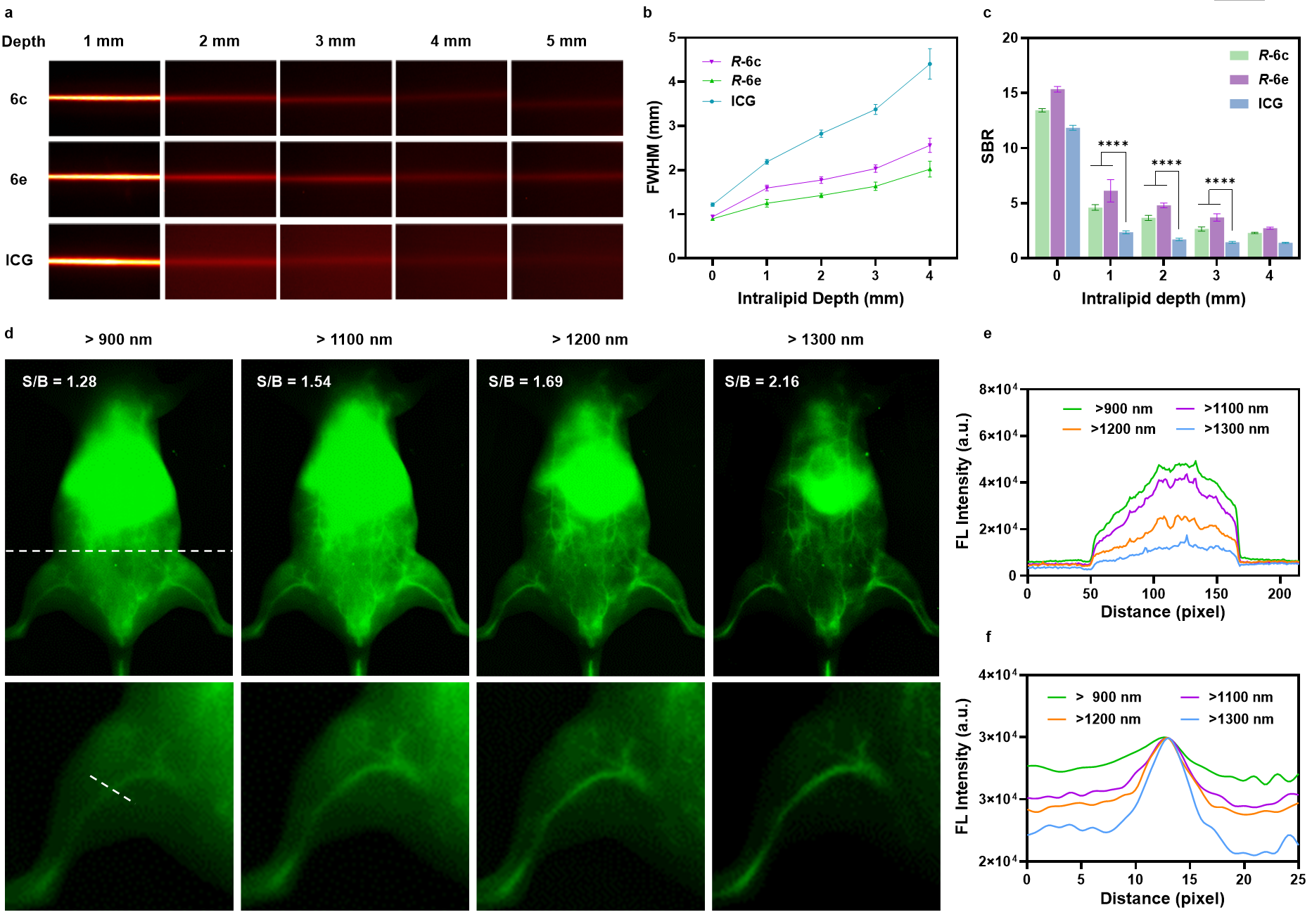
图5 NIR-II区域的高性能活体成像表现
该研究建立了高效构建硼手性BODIPY的方法,快速获得一系列具有近红外甚至近红外二区发射的荧光探针。这些染料不仅在细胞中表现出明确的手性选择性定位,还在小鼠血管成像中实现了高分辨率、低背景的成像效果,为开发新型精准诊断与活体成像工具提供了可靠策略和分子基础。随着硼手性BODIPY库的建立,以及相关光物理性质、细胞行为与体内成像机制的逐步清晰,这一体系将成为跨学科合作的坚实基础。
该研究以"Streamlined construction of boron-stereogenic BODIPY library for near-infrared bioimaging"为题发表在Nature Communications上。本项工作由南方科技大学化学系/深圳格拉布斯研究院何川团队与北京大学深圳医院/精准医学研究院穆婧团队联合完成。论文第一作者为赵佳怡、任李庆与蓝德仁。工作获得国家自然科学基金、广东省催化重点实验室、深圳市科创委等项目支持。